Методы медицинской визуализации часто помогают успешно диагностировать и лечить злокачественные новообразования. В частности, магнитно-резонансная томография (МРТ) широко используется благодаря своему высокому разрешению, особенно при применении контрастных веществ.
В новом исследовании, опубликованном в журнале Advanced Science, сообщается о новом самосворачивающемся наноразмерном контрастном веществе, которое может помочь более детально визуализировать опухоли с помощью МРТ.
Что такое контраст?СМИ?
Контрастные вещества (также известные как контрастные препараты) — это химические вещества, которые вводятся (или принимаются) в ткани или органы человека для улучшения качества изображения. Эти препараты имеют более высокую или более низкую плотность, чем окружающая ткань, создавая контраст, который используется для отображения изображений с помощью некоторых устройств. Например, препараты йода, сульфат бария и т. д. обычно используются для рентгеновского наблюдения. Они вводятся в кровеносный сосуд пациента с помощью шприца с контрастным веществом под высоким давлением.
На наномасштабе молекулы сохраняются в крови в течение длительного времени и могут проникать в солидные опухоли, не вызывая специфических для опухоли механизмов уклонения от иммунного ответа. Несколько молекулярных комплексов на основе наномолекул были изучены в качестве потенциальных носителей CA в опухоли.
Эти наноразмерные контрастные вещества (НКВ) должны быть правильно распределены между кровью и исследуемой тканью, чтобы минимизировать фоновый шум и достичь максимального отношения сигнал/шум (S/N). При высоких концентрациях НКВ дольше сохраняются в кровотоке, что увеличивает риск развития обширного фиброза из-за высвобождения ионов гадолиния из комплекса.
К сожалению, большинство используемых в настоящее время нанокомпозитных агентов содержат совокупности нескольких различных типов молекул. Ниже определенного порогового значения эти мицеллы или агрегаты имеют тенденцию к диссоциации, и последствия этого процесса остаются неясными.
Это вдохновило на исследования самосворачивающихся наноразмерных макромолекул, не имеющих критических порогов диссоциации. Они состоят из жирового ядра и растворимого внешнего слоя, который также ограничивает перемещение растворимых единиц по контактной поверхности. Это может впоследствии повлиять на параметры молекулярной релаксации и другие функции, которыми можно манипулировать для улучшения доставки лекарств и специфичности in vivo.
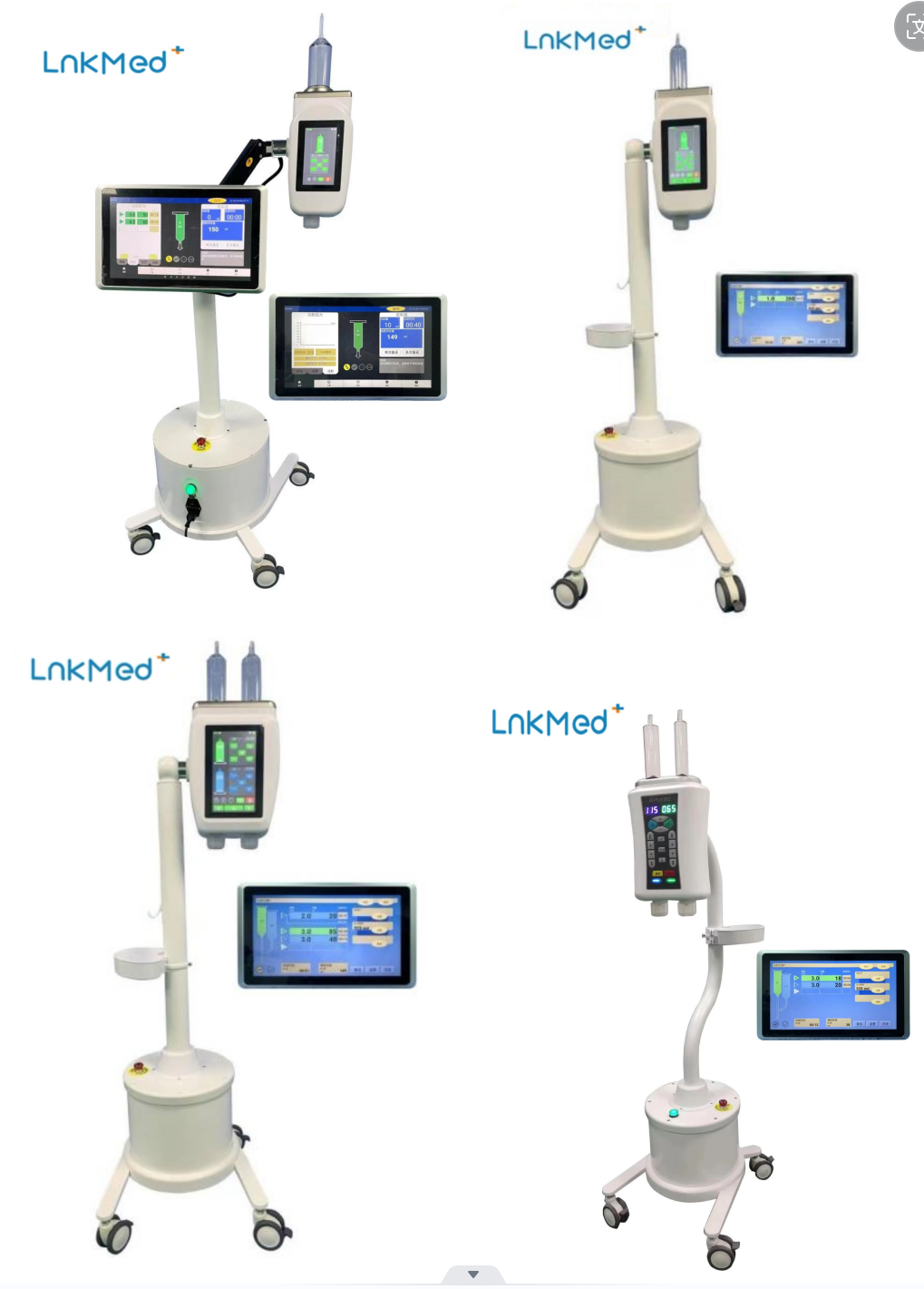
Контрастное вещество обычно вводится в организм пациента с помощью инжектора контрастных веществ под высоким давлением.LnkMedКомпания, профессиональный производитель, специализирующийся на исследованиях и разработке инъекторов контрастных веществ и сопутствующих расходных материалов, продала свой бизнес.CT, МРТ, иДСАНаши форсунки пользуются признанием на рынке многих стран как в России, так и за рубежом. Наш завод может обеспечить всю необходимую поддержку.расходные материалыВ настоящее время пользуется популярностью в больницах. Наш завод применяет строгие процедуры контроля качества при производстве продукции, обеспечивает быструю доставку и комплексное и эффективное послепродажное обслуживание. Все сотрудникиLnkMedНадеемся в будущем активнее участвовать в развитии индустрии ангиографии, продолжать создавать высококачественную продукцию для клиентов и оказывать помощь пациентам.
Что показывают результаты исследования?
В методе NCA внедрен новый механизм, который усиливает продольное релаксационное состояние протонов, позволяя получать более четкие изображения при значительно меньших концентрациях комплексов гадолиния. Меньшая концентрация снижает риск побочных эффектов, поскольку доза контрастного вещества минимальна.
Благодаря свойству самосворачивания, образующийся SMDC имеет плотное ядро и сложную, тесную среду. Это повышает релаксационную способность, поскольку внутреннее и сегментарное движение вокруг границы раздела SMDC-Gd может быть ограничено.
Этот нейтронный углеродный агент может накапливаться в опухолях, что позволяет использовать нейтронно-захватную терапию с гадолинием для более специфичного и эффективного лечения опухолей. До настоящего времени это не было достигнуто в клинической практике из-за недостаточной селективности доставки 157Gd к опухолям и поддержания их концентрации на должном уровне. Необходимость введения высоких доз связана с побочными эффектами и плохими результатами лечения, поскольку большое количество гадолиния, окружающего опухоль, защищает ее от воздействия нейтронов.
Наноразмерные структуры обеспечивают избирательное накопление терапевтических концентраций и оптимальное распределение лекарственных препаратов внутри опухолей. Молекулы меньшего размера могут выходить из капилляров, что приводит к повышению противоопухолевой активности.
«Учитывая, что диаметр SMDC составляет менее 10 нм, наши результаты, вероятно, обусловлены глубоким проникновением SMDC в опухоли, что помогает им избежать экранирующего эффекта тепловых нейтронов и обеспечивает эффективную диффузию электронов и гамма-лучей после облучения тепловыми нейтронами.«
Каковы последствия?
«Может способствовать разработке оптимизированных SMDC для улучшения диагностики опухолей, даже когда требуется несколько инъекций МРТ».
«Наши результаты подчеркивают потенциал тонкой настройки NCA посредством самосворачивающегося молекулярного дизайна и знаменуют собой значительный прогресс в использовании NCA в диагностике и лечении рака».
Дата публикации: 08.12.2023